一款由本地注资和参与研发的冠病疫苗,已经完成对580名美国和本地受试者的第二期临床试验,九成在注射一剂疫苗的28天后产生了抗体,免疫T细胞也比其他信使核糖核酸疫苗高出8倍至16倍。公司准备在高风险地区开展第三期临床试验,并备产1000万剂疫苗,预计年底获紧急批准后就可投放市场。
美国生物科技公司Arcturus Therapeutics总裁兼首席执行官约瑟夫·佩恩(Joseph Payne)通过越洋视讯接受《联合早报》专访时,介绍这款名为ARCT-021疫苗的最新进度。
他说,第二期临床试验有106人来自新加坡,他们从未感染冠病。第二期结果显示,疫苗安全性和效能和第一期相似,注射一剂5微克疫苗的28天后,大多数受试者都能测出抗体。
ARCT-021疫苗由这家纳斯达克上市公司和杜克—新加坡国立大学医学院合作研发,并获新加坡经济发展局4500万美元资助。
他说:“根据杜克—国大医学院研究,比起辉瑞(Pfizer-BioNTech)和莫德纳(Moderna)的信使核糖核酸(mRNA)疫苗,ARCT-021疫苗有自我复制的能力,注射者体内免疫T细胞比其他mRNA疫苗高出8倍至16倍。这项技术也能比较准确地模拟病毒的入侵,因此让注射者有更强的免疫反应。”
至于更强的T细胞反应是否能提供更强烈或是更持久的保护,甚至能对抗变种毒株,公司还在研究。佩恩也解释,mRNA技术的好处是这种基因组成部分可以人造,可根据变种毒株调整mRNA的基因表达,从而达到刺激人体对变种毒株产生反应的效果。
由于美国的接种已上轨道,公司得另找病毒仍然肆虐的国家展开第三期临床试验,这样才能在接种和无接种人群之间作染病比率的对比。
佩恩透露,他们把目标投向拉丁美洲、东欧、中东和东南亚等地区,一旦取得批准,就马上对外公布试验地点。
第三期临床试验预计需要1万5000人。根据计算,一个国家冠病发病率若是1%,临床试验需要三个半月。佩恩指出,一些国家的发病率达到4%,试验有望能以快四倍的时间进行,并在一个月内完成。一旦有了安全性和效用数据,公司会立即申请紧急批准。
公司已完成1000万剂疫苗的生产,除了将用于第三期临床试验,也准备在获得紧急批准后,马上推出市场。
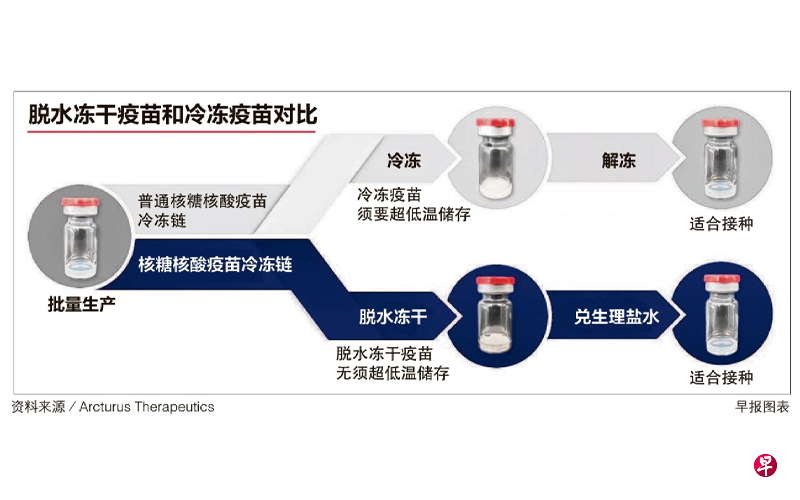
冻干技术制成粉末状态 无需低温也能长期保存
这款疫苗以冻干(lyophilised)技术制成粉末状,无需低温就能长期保存,接种时才兑生理盐水,一瓶可以注射15至20剂。这样一来,不但便于储存和冷链运输,也可大规模接种。
虽然疫苗研发落后于其他主要疫苗厂商九个月,但佩恩认为疫苗具有后发优势,能根据现有疫苗的经验和不足之处进行调整,包括只须要注射一剂。
他也说:“和其他疫苗相比,这款疫苗的聚乙二醇脂质保护层较少,也是唯一会在人体中自动降解的疫苗,因此不良反应相信会比其他疫苗少。”
虽然美国和新加坡预计能在年底之前完成疫苗接种工作,但佩恩也认为,世界上有许多国家仍需大量的疫苗供应,就算是在已经开始注射的国家,许多因过敏反应不适合接种其他疫苗的人也能使用。
至于那些使用灭活疫苗的国家,他也认为mRNA疫苗能提供更好的免疫保护。